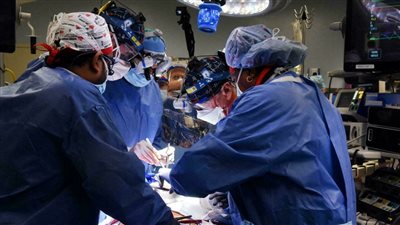
لأول مرة.. زراعة "ناجحة" لكلية خنزير في جسم بشري
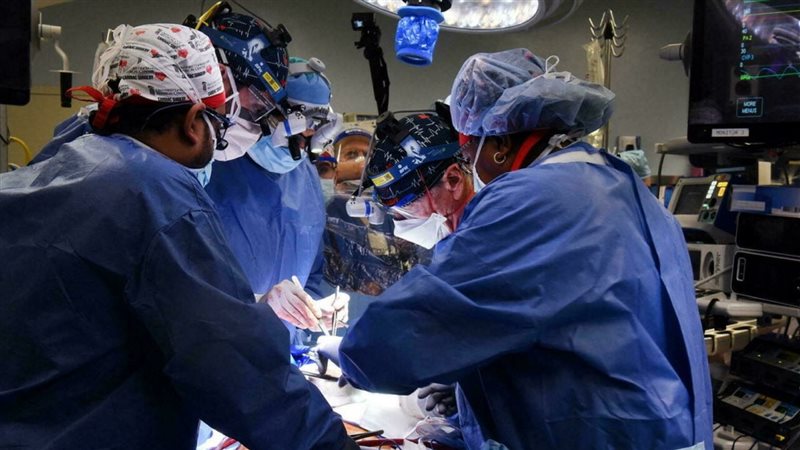
بعد أيام من إعلان نجاح عملية زراعة قلب خنزير في قلب مريض أمريكي، أعلن العلماء عن نجاح عملية زرع كليتين من خنزير معدَّل وراثيًّا في متلق بشري، ووجدوا أن الأعضاء تنتج البول ولم يتم رفضها خلال التجرِبة التي استمرت أيامًا.
وأجريت العملية لمريض ميت دماغيًّا وكان متبرعًا مسجلًا بالأعضاء، وأجازت عائلته البحث، وفقًا للدراسة الجديدة، التي نشرت أمس الخميس، في المجلة الأمريكية للزراعة.
تجارب إكلينيكية رسمية
ويعتزم فريق البحث في نهاية المطاف زرع كلى خنازير في المرضى الأحياء، في تجارِب إكلينيكية رسمية، لكنهم أرادوا أولًا معالجة بعض أسئلة السلامة الحرجة.
وأعلنت كلية الطب بجامعة ألاباما في برمنجهام أمس عن أول بحث تمت مراجعته من قبل الأقران يحدد عملية الزرع الناجحة لكلى الخنزير المعدَّل وراثيًّا من الدرجة السريرية إلى شخص ميت دماغيًّا، لتحل محل الكلى الأصلية للمستضيف.
وتوضح هذه النتائج الإيجابية كيف يمكن أن يَعالج زرع الأعضاء أزمة نقص الأعضاء في جميع أنحاء العالم.
وفي الدراسة، اختبر العلماء أول نموذج قبل سريري بشري لزرع كلى خنزير معدَّل وراثيًّا في البشر، وحصل العلماء على الأعضاء من خنزير معدل وراثيا في بيئة خالية من مسببات الأمراض.
إنجازا للبشرية
وقال سيلوين فيكرز، عميد كلية الطب بجامعة ألاباما والمدير التنفيذي لنظام الصحة بالجامعة: "تعد نتائج اليوم إنجازًا رائعًا للبشرية وتقدم زراعة الأعضاء في المجال السريري، ومع هذه الدراسة أثبتت فرق البحث لدينا أيضًا أن النموذج المتوفَّى لديه إمكانات كبيرة لدفع مجال زرع الأعضاء إلى الأمام".
ولأول مرة، تم أخذ كلى الخنازير المزروعة من خنازير تم تعديلها وراثيًّا بعشرة تعديلات جينية رئيسية ما جعل الكلى مناسبةً للزرع في البشر.
وتوضح هذه العملية الجدوى طويلة المدى للإجراء، وكيف يمكن أن تسير عملية الزرع في العالم الحقيقي.
وتحمل الخنازير ستة جينات إضافية مأخوذة من الجينوم البشري: أربعة للمساعدة في جعل أعضاء كل خنزير تبدو مألوفة أكثر لجهاز المناعة البشري واثنين لمنع تكوين جلطات الدم.
بعد استخراج الكلى من الخنزير المتبرع به، قام الفريق بفحص الأعضاء، لاحظ الفريق عمومًا أن كلى الخنازير تشبه كلى الإنسان، لكنها اختلفت في بعض النواحي.
ووجد العلماء، بعد إجراء الزراعة، أن الكلى المزروعة ترشح الدم وتنتج البول والأهم من ذلك أنها لم تُرفض على الفور، وكانت الكلى قادرةً على البقاء حتى انتهاء الدراسة، بعد 77 ساعة من الزرع.
وبعد الزرع، أظهرت الكلى اليمنى في البداية إنتاج بول "قوي"، بينما أنتجت الكلية اليسرى كمية أقل بكثير من البول، ولاحظ المؤلفون أن سبب هذا الاختلاف غير معروف، ولكن قد يكون مرتبطا بكيفية عمل كل عضو في البداية من الخنزير المتبرع.
ومقارنة بالكلية اليمنى، أمضت الكلية اليسرى وقتا أطول في درجة حرارة الغرفة بعد انقطاعها عن إمداد دم الخنزير وقبل وضعها على الثلج.
وكتب المؤلفون أن هناك حاجة إلى مزيد من البحث لمعرفة كيف يمكن لهذه العوامل أن تضعف وظيفة عضو خنزير في الإنسان المتلقي.
مستوى الكرياتينين
وعلى الرغم من أن الكليتين تنتجان البول، وإن كان بكميات مختلفة، لم يقم أي من العضوين بترشيح الفضلات من الدم مثل الكلى التي تعمل بكامل طاقتها.
ووجد الفريق أن مستوى الكرياتينين، وهو منتج نفايات لوظيفة خلايا العضلات، في الدم لم ينخفض بمرور الوقت، ولم تفرز أي من الكليتين الكرياتينين المهم في البول.
وأشار العلماء إلى أنه من غير الواضح ما إذا كان هذا الخلل ناجما عن تلف في الكلى، أو كان مرتبطا بالتغيرات الفسيولوجية التي يسببها الموت الدماغي.
وقال جايمي لوك، مدير معهد زراعة الأعضاء الشامل، ورئيس الجراحين: "تمثل هذه اللحظة التي تغير قواعد اللعبة في تاريخ الطب نقلة نوعية وعلامة فارقة في مجال زراعة الأعضاء، والتي يمكن القول إنها أفضل حل لأزمة نقص الأعضاء".
وأضاف: "لقد قمنا بسد الفجوات المعرفية الحرجة وحصلنا على بيانات السلامة والجدوى اللازمة لبدء تجربة إكلينيكية على البشر الأحياء المصابين بمرض الفشل الكلوي في المرحلة النهائية".
وشرح لوك: "بيئة موت الدماغ معادية تماما، ما يجعل تقييم وظائف الكلى أمرا صعبا". وعلى مدار التجربة، بدأت أعضاء المريض بالفشل، وتطور تخثر دم غير طبيعي، وأصبح دمه أيضا أكثر حمضية بسبب تراكم أيونات الهيدروجين.
واستخدم العلماء العديد من الأدوية والحقن لمواجهة آثار موت الدماغ أثناء الدراسة، لكن مع ذلك، ربما تكون التأثيرات قد قوضت وظيفة كلى الخنازير، وفقا للورقة البحثية.
ويبلغ العمر الطبيعي للخنزير 30 عاما، ويمكن تربيته بسهولة ويكون له أعضاء بنفس الحجم لدى الإنسان.
ووقع اختبار كلى الخنازير المعدلة وراثيا على نطاق واسع في الرئيسيات غير البشرية. وبالإضافة إلى الاختبار في الرئيسيات غير البشرية، فإن تقييم كلى الخنازير المعدلة وراثيا في بحث نموذج ما قبل سريري بشري قد يوفر معلومات مهمة حول السلامة والفعالية المحتملة للكلى في متلقي الزراعة البشرية، بما في ذلك التجارب السريرية.
وتابع لوك: "هذا النموذج قبل السريري البشري هو وسيلة لتقييم سلامة وجدوى نموذج الرئيسيات من الخنزير إلى غير البشر، دون المخاطرة بإنسان حي. وتوضح دراستنا أنه قد تم التغلب على العوائق الرئيسية التي تحول دون زرع الأعضاء البشرية، وتحدد أن هناك حاجة إلى معرفة جديدة لتحسين نتائج زرع الأعضاء في البشر، وتضع الأساس لإنشاء نموذج بشري جديد قبل السريري لمزيد من الدراسة".
وتأتي التجربة بعد أيام فقط من إعلان أطباء نجاح عملية لرزع قلب خنزير في جسم مريض بشري.
وجرت الجراحة التجريبية، التي وصفت بأنها ناجحة، في مركز ميريلاند الطبي بجامعة ميريلاند بالولايات المتحدة، ليصبح ديف بينيت، 57 عاما، أول شخص في العالم يعيش بقلب خنزير.
وكان العلماء في دول عدة قد بدأوا خلال الأعوام الماضية تركيز أبحاثهم على الخنازير لمعالجة مشاكل المرضى الذين يحتاجون إلى أعضاء بشرية لإنقاذ حياتهم، ومن أهم العقبات التي كانت تواجههم هي نوعية السكر الموجود في خلايا الخنزير الذي يرفضه جسم الإنسان بشكل فوري، ولكن التجربة الواعدة نجحت بفضل استخدام كلية لحيوان معدل جينيا وخلاياه خالية من ذلك السكر المعروف باسم "سكر ألفا-جال".
وبشكل عام، تشير الدراسة إلى أنه في حين تم التغلب على العديد من العوائق التي تحول دون زراعة الكلى من خنزير إلى إنسان، فإن العديد من الأسئلة حول الإجراء لا تزال دون إجابة.
ويمكن أن توفر الدراسات المستقبلية على المتوفين دماغيا بعض الإجابات عن هذه الأسئلة، بينما قد يحتاج البعض الآخر إلى التحقيق في الرئيسيات غير البشرية. وفي النهاية، سيتم تناول بعض الأسئلة في التجارب السريرية على البشر الأحياء.